
AsitBazlar ASİT VE BAZLARIN ÖZELLİKLERİ
İçindekiler17- ASİTLER ve BAZLAR 66517-1 Asit ve Baz Tanımı-Arrhenius- Kuramı:Sunuş17-2 Asit ve Baz Tanımı Bronsted-Lowry Kuramı17-3 Suyun İyonlaşması ve pH Eşeli17-4 Kuvvetli Asitler ve Bazlar17-5 Zayıf Asitler ve Bazlar17-6 Çok Protonlu Asitler17-7 Asit ve Baz Özelliği Gösteren İyonlar17-8 Molekül Yapısı ve Asit-Baz Davranışı17-8 Lewis Asit ve BazlarıÖzel Konu.

8.SINIF 4.ÜNİTE ASİTLER VE BAZLAR FENOZOM
Bu ünite hakkında: Bu ünitede, asit-baz kimyasında kimyasal dengenin rolü işlenir. pH ve pOH, zayıf asit ve bazlar, tamponlar, asit-baz titrasyonları ve daha fazlası hakkında bilgi edinin. 70'in üzerinde AP uyumlu soru ile öğrendiklerinizi pekiştirin ve AP Kimya sınavına hazırlanın.

8.2 ASİT BAZ VE PH ÇİZELGESİ CANLI YAYIN TEKRARI YouTube
• Bazlar asitler ile nötralleşme tepkimesi verir. • Bazlar amfoter metallerle (Al,Cr,Zn,Sn,Pb,Be) reaksiyona girerek hidrojen gazı açığa çıkarır. ASİT VE BAZLARIN İNDİKATÖRLERE ETKİSİ • Bir maddenin asit veya baz oluşuna bağlı ola-rak renk değiştiren maddelere indikatör (belir-teç) denir

Asitler ve Bazlar / Püf Noktaları ile Detaylı Anlatım 🧪 8.Sınıf Fen
öğreneceksiniz. Asit ve bazlar yaşamın olduğu çoğu alanda bulunur ve kontrolden çıkmadıkça yararlıdırlar. İnsan vücudu kontrolün bozulmaması için vücudun pH seviyesini istenen düzeyde tutmaya çalışır. Soluduğumuz havanın kalitesi de vücudun pH dengesini sağlamak için önemlidir. Günümüzde havaya salınan asidik.

Asitler Ve Bazlar Konu Anlatımı Nedir
Asitler, Alkaliler Ve Tuzlar. 37690 okunma. Günlük Hayatta Kullandığımız Asit ve Bazlar hayatımızda kullandığımız hemen hemen tüm gerekli şeylerin içinde yer almaktadır. Olumlu yönleri olduğu gibi olumsuz etkileri de barındırabilen asit ve bazlar, sabun, çamaşır suyu, tuz ruhu, gazoz, sirke ve bazı ilaçların.

Asit ve Bazların Özellikleri (Farkları) Nelerdir? Eğitim
PH Nedir(Asitler ve Bazlar) Bilim adamları pH ölçeğini kullanarak asitleri ve bazları takip ederler. Açılımı "Power of Hydrogen" (Hidrojenin Gücü)'dir. 1909'da Danimarkalı biyokimyacı Sören Sörensen asitliği ölçmek için pH ölçeğini icat etti . PH ölçeği aşağıdaki formülle tarif edilir: pH = -log [H.

8.SINIF ASİTLER VE BAZLAR YouTube
Asit - baz kavramları, asit - bazların genel özellikleri ve nötrleşme olayı detaylıca anlatılmıştır. Asitler ve bazlar suyla çözeltilerinde iyon veren maddelerin bütünüdür. Günlük hayatta kullandığımız sabun, deterjan, deodorant, temizlik maddeleri, elma, sirke, limon, üzüm ve zeytinyağı gibi daha birçok şey.

Asit ve bazlar çalışma kağıdı ve cevap anahtarı
Asitler ve Bazlar (Acids and Bases)1. Bronsted-Lowry Asit-Baz Tanımı (Brønsted-Lowry Acids and Bases )2. Lewis Asit- Baz Tanımı (Lewis AcIds And Bases)Örnekl.

Asit Baz Özellikleri ve Ayırt Edilmesi Bikifi
Asit ve Bazların Tahribatları Asitler ve bazlar tahriş edici (aşındırıcı) özelliğe sahiptir. Asit ve bazları kullanırken, taşırken dikkatli olmamız gerekir. Laboratuvar, mutfak, banyoda kullanılan asit ve bazların etkilerinden korunmak için eldiven takılmalı, gözlük kullanılmalıdır.

Asitler Bazlari Afişi
Asitler ve Bazlar Afişi (Posteri) Ürün Kodu: fteog12. Marka: okulcenter. Stok: 20+. 50,00 TL. 4,17 TL 'den başlayan taksitlerle. Malzeme Çeşidi Seçiniz: Yapışkanlı Folyo Vinil Branda Dekota (3mm kalınlığında plastik) Ürün Boyutunu Seçiniz:
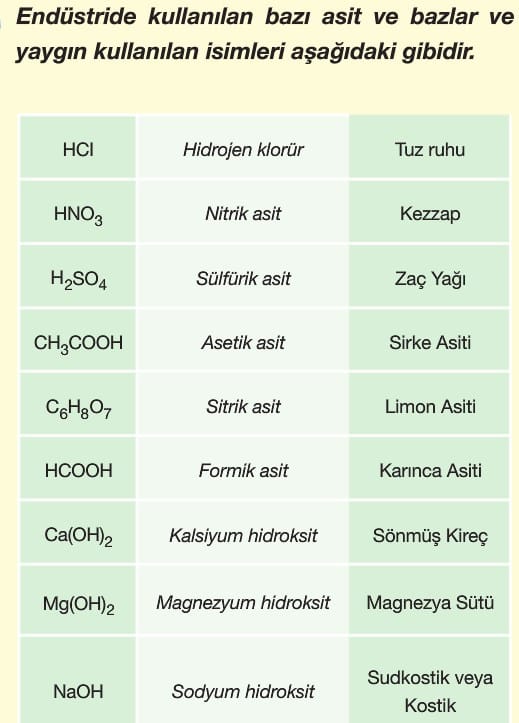
Asit ve Bazların Kullanım Alanları Özellikleri Kimya Tyt Konu
Asit ve bazlar ile ilgili poster çalışması. Asitler ve bazlar ile ilgili poster hazırlamak için öncelikle asitler ve bazların temel özelliklerini kullanman gerektiğini bilmelisiniz. Asitlerin ve bazların aşağıda verdiğimiz özelliklerini posterlerde kullanabilirsiniz. Aşağıda yine verdiğimiz resimleri de posterlerin için.

PPT Asitler ve Bazlar PowerPoint Presentation, free download ID5357288
pH, pOH ve pH ölçeği. Brønsted-Lowry Asit Baz Kuramı (Teorisi) Asit ve Bazların Bronsted-Lowry Tanımı. Suyun Otoiyonizasyonu. Suyun Otoiyonizasyonu ve Kw. pH Nedir? Kuvvetli Asit Çözeltileri. Kuvvetli Baz Çözeltileri. Asit Kuvveti, Anyon Hacmi ve Bağ Enerjisi.
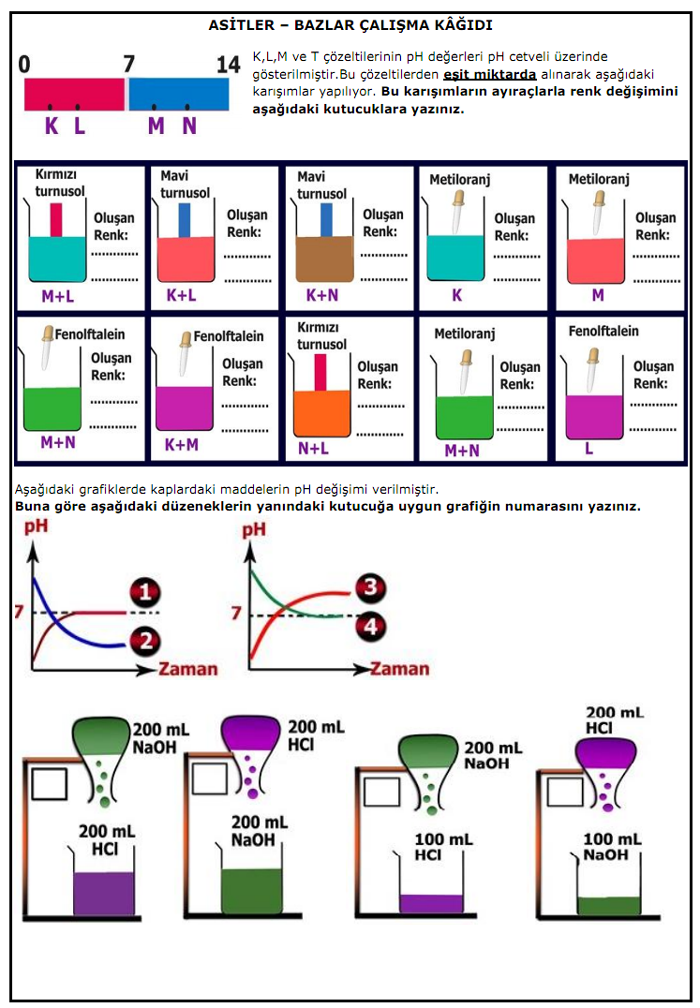
Asit ve bazlar çalışma kağıdı ve cevap anahtarı
Asitler Bazlar ve Tuzlar Asit Nedir; Sulu çözeltilerinde hidrojen iyonu (H+) verebilen maddelere denir. Mesela hidroklorik asit olan HCL suda çözününce H+ Cl elde edilir. Yani H+ iyonu meydana gelmiş olur. İşte bu maddelerin özellikler şunlardır; Sudaki çözeltilerine H+ iyonu verirler. Seyreltik çözeltilerinin tadı ekşidir.
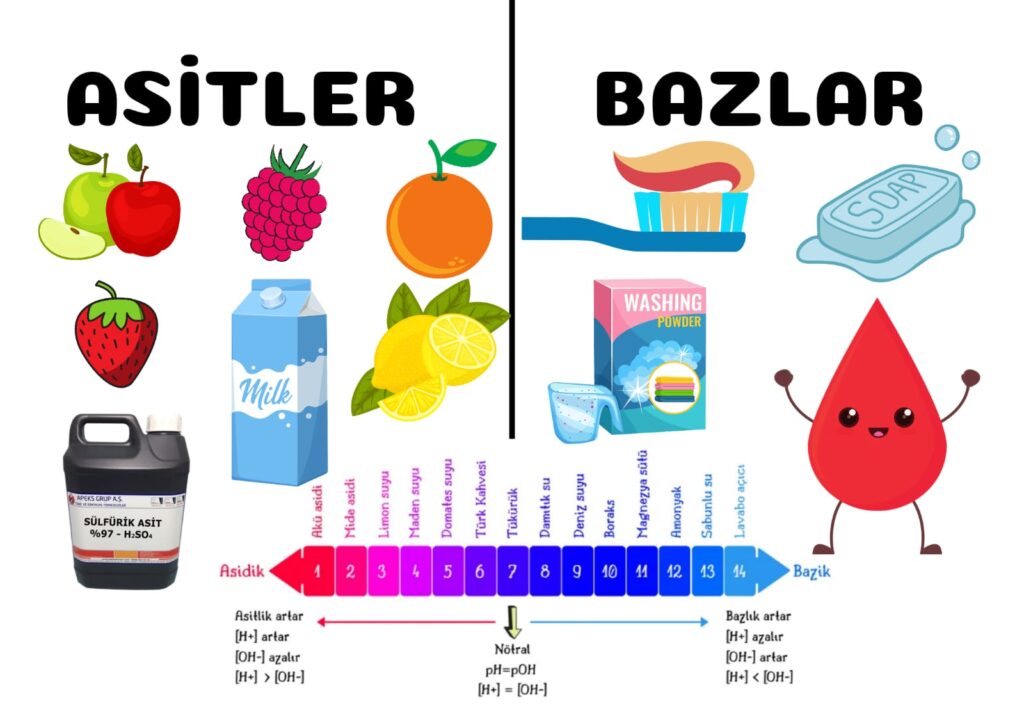
8.SINIF FEN BİLİMLERİ POSTERLERİ FENUS BİLİM
Çevremizdeki pek çok maddeyi ortak kimyasal özelliklerine göre gruplandırabiliriz. -. Asitler, bazlar ve tuzlar bu. Folik asit gruplardan üçünü oluşturur. Asitler. Asit kelimesi latince "ekşi" anlamına gelir. Ekşi tat veren maddeler asit özelliğine sahiptir. limonda sitrik asit elmada malik asit.
Asit ve bazlar 2
8. Sınıf Asitler ve Bazlar Konu Anlatımı💻 https://www.derslike.com📱 https://www.instagram.com/derslike/Artık herkes DersLike kanalında! Sen de aramıza.

8 Sınıf Asitler ve Bazlar (Animasyonlu ve Detaylı Anlatım) En doğru
Asit (H +) ve baz (OH -) tepkimeye girerek tuz ortaya çıkmasına neden olurlar. Asit + Baz → Tuz + H2O. Bu durum nötrleşme olarak ifade edilmektedir. Asit maddesinden gelen H + iyonlarının mol sayısı (n) ile baz maddesinden gelen OH- iyonlarının mol sayısı eşitse ortam nötr hale gelir ve pH seviyesi 7 olarak belirlenir.